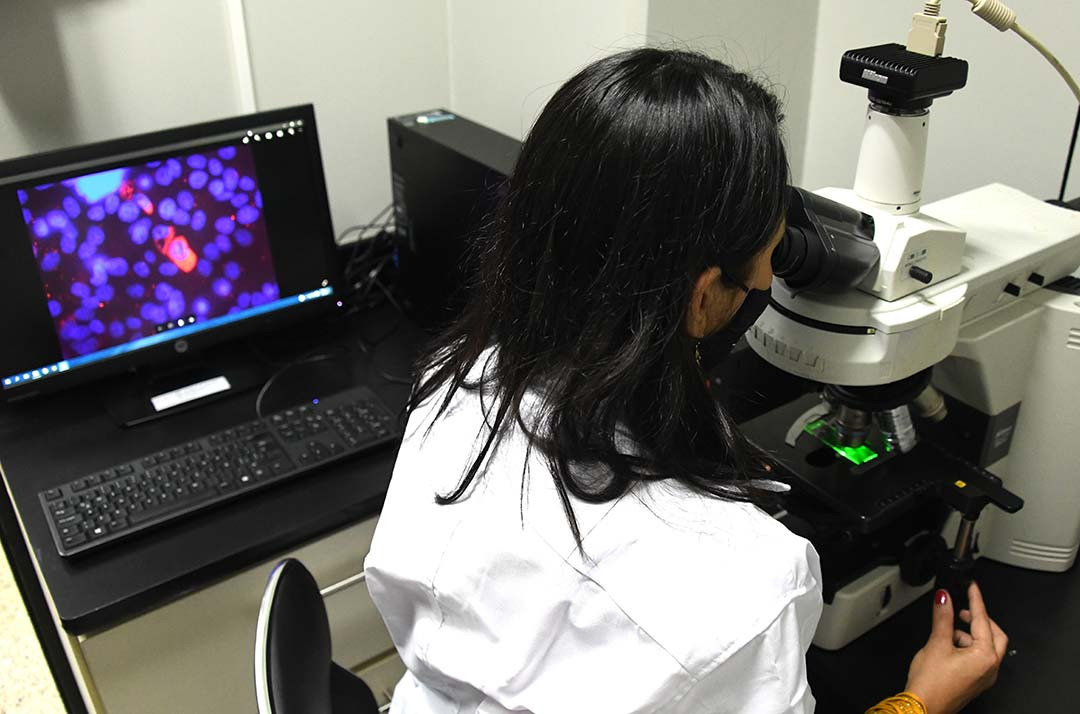
“Una investigación muy notable, con datos convincentes y mediante un experimento bastante inteligente”. De esta manera Vincent Racaniello, uno de los científicos integrantes de la prestigiosa Sociedad Americana de Microbiología (ASM por sus siglas en inglés), resaltó el estudio liderado por Pamela Altamirano Silva; una joven científica costarricense de tan solo 36 años de edad.
Esta talentosa mujer, quien es docente e investigadora de la Facultad de Microbiología de la Universidad de Costa Rica (UCR)― y efectuó el estudio de la mano con otros siete científicos de la UCR y de la Universidad Nacional (UNA)― fue la encargada de llevar a cabo uno de los diversos análisis sobre brucelosis desarrollados en el país. Esta vez, enfocado en hallar el porqué la respuesta molecular de la bacteria aumenta su potencial infeccioso.
Los cumplidos a su sobresaliente trabajo se realizaron vía podcast en un segmento de alcance internacional llamado “Esta Semana en Microbiología”, auspiciado por la ASM.
Dicha asociación es la más prestigiosa del continente americano en el campo de la microbiología desde 1899. Por lo tanto, las palabras que utilizó tanto el Dr. Racaniello, como los otros dos científicos destacados que también lo acompañaron en el podcast, Michele Swanson y Michael Schmidt, son contundentes y claros para mostrar un imponente hecho.
Los resultados logrados por Pamela y su equipo de científicos de la UCR son trascendentales ante una bacteria altamente infecciosa, de gran peligro para el ganado y hasta para el mismo ser humano. ¿Su nombre científico? Brucella abortus.
“Lo que es tan notable en la investigación, es que te convencen de que el crecimiento intracelular de alguna manera influye en la programación de la bacteria, ¡tanto!, que dicha programación la hace más capaz de interactuar con nuevas células hospedero para replicarse. En otras palabras, la bacteria genera una transmisión más eficiente a la siguiente nueva célula hospedera. Lo destacado en el estudio es el modelo que propusieron para demostrarlo, el cual es bastante extraordinario”, comentó Vincent Racaniello.
En lo mismo coincidió la Dra. Swanson, quien hizo hincapié a que “la parte más importante del estudio de la primera autora, Pamela Altamirano, es el desarrollo minucioso de un ensayo (modelo) a fin de extraer las bacterias intracelulares de las células ya infectadas, y luego caracterizarlas químicamente para medir su capacidad de invadir la siguiente célula. Esto fue verdaderamente ingenioso y Pamela es una científica realmente apasionada”, afirmó la estadounidense.
Puede escuchar el podcast de los expertos estadounidenses aquí:
Desde la voz de Pamela, el reconocimiento alcanzado es muy motivante, porque es el resultado de horas de esfuerzo y de un trabajo en equipo enfocado en dar respuesta a interrogantes que siguen inquietando al mundo de la ciencia, mismo que puede resumirse de la siguiente manera: ¿cómo un microorganismo tan pequeño puede causar un daño tan grande?
“Lograr esa mención es muy gratificante. Primero, porque soy 100 % sello UCR y, segundo, porque la ciencia no es fácil, requiere de mucha persistencia y a veces es frustrante cuando no se obtiene un resultado a la primera. Se necesita de mucho sacrificio a nivel personal. Había veces que tenía que cuidar a mi hija y entonces hacíamos picnics en la UCR durante los tiempos de incubación de la bacteria. Así compartía con ella e iba sacando el proyecto adelante. Entonces, al final uno dice: ¡valió la pena!”, compartió Altamirano.

“Desde niña siempre me imaginé en un laboratorio investigando este mundo microscópico que pocos conocen y que puede desencadenar enfermedades en las personas. El poder dar un aporte en este campo, acompañada de científicos con gran trayectoria, es realmente alentador”, mencionó Pamela Altamirano.
Karla RichmondEl estudio
Pero, ¿por qué este estudio es tan importante que, incluso, asombró a un riguroso panel de expertos internacionales? La razón es sencilla: es el primero que logra explicar cómo el patógeno aumenta su capacidad para multiplicarse en nuevas células hospederas.
El hallazgo da pistas invaluables a la comunidad científica internacional, pues sirven como insumos para abordar una bacteria causante de una enfermedad fuertemente contagiosa conocida como Brucelosis. Dicha enfermedad puede llegar a enfermar al ser humano y a los animales de producción, principalmente, al ganado bovino.
Si alguno de los animales presenta la bacteria, es muy probable que sea sacrificado para evitar que se expanda al resto de la manada y llegue a contagiar a alguna persona.
En un ser humano, la brucelosis se manifiesta mediante fiebres ondulantes, con otros síntomas como la fatiga, que pueden presentarse a través de años e incluso décadas. En algunos casos, el patógeno desencadena complicaciones severas como meningoencefalitis, espondilitis, artritis y endocarditis.
“La Brucella abortus es una bacteria intracelular. ¿Qué quiere decir esto? Que es un patógeno que necesita de otra célula para multiplicarse y así mantener su ciclo de vida. Esta bacteria se puede multiplicar fuera de las células, pero prefiere vivir dentro de ellas. Entonces, el sistema que estudiamos interviene en el paso que efectúa la bacteria desde un ambiente fuera de las células hacia el interior de las células (de fuera hacia dentro). También, en la transición desde un ambiente adentro de las células hacia un ambiente fuera de las células (de adentro hacia fuera). Aquí interviene el sistema que analizamos, pues activa una respuesta molecular en la bacteria que le genera una mejor capacidad para sobrevivir, adherirse y multiplicarse”, comentó Altamirano.
Este trabajo es la continuación de un esfuerzo anterior desarrollado en el 2018. Durante ese año, se ejecutó una investigación que dio la posibilidad de explicar los dos componentes claves de la B. abortus. Uno es una proteína sensora que detecta señales y el otro es una proteína reguladora con la misión de enviar respuestas a nivel de expresión de genes cuando el sensor le notifica que algo está pasando.
“Con el estudio del 2018 nos habíamos enfocado en cómo ese sistema de la bacteria le avisa que está entrando a una célula a infectar. Es decir, en hallar cómo es que la bacteria entiende que está experimentando una transición de fuera hacia dentro de la célula. Es un sistema con el que la bacteria dice ‘OK, voy entrando a una célula. Ahora, necesito activar una serie de señales. Con estas señales podré expresar los genes que me permitirán sobrevivir dentro de la célula en la cual me voy a multiplicar’. Ahora, en este nuevo estudio (2021) es a la inversa; cómo la bacteria va a salir de la célula infectada para contagiar a otras”, ahondó Altamirano.
De acuerdo con la científica, cuando la bacteria empieza a salir de la célula que ya infectó, su sistema registra que nuevamente está cambiando de ambiente.
Como resultado, se va a desencadenar respuestas que favorecen a que el patógeno salga por completo de la célula infectada de una forma más competente. Posteriormente, activa una serie de sistemas especializados para infectar nuevas células y adherirse a ellas con mayor eficiencia. ¿Su objetivo? Iniciar un nuevo ciclo de infección.
Un arduo esfuerzo
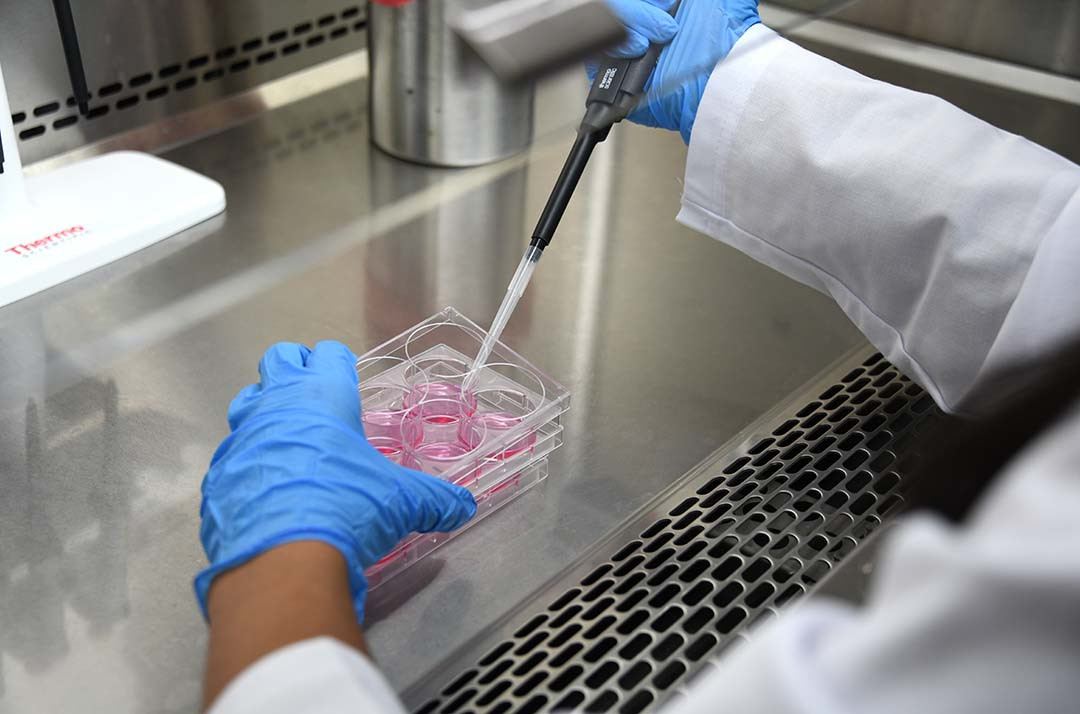
Los avances que hoy se obtienen son el resultado de más de siete años de esfuerzo, que iniciaron desde la estandarización de un protocolo para purificar las bacterias intracelulares.
Así, con el protocolo estandarizado, el equipo de la UCR procedió a infectar células en cultivo para recrear todo el ciclo celular. Posteriormente, extrajeron los microorganismos dentro de las células después de 48 horas de incubación y las utilizaron para iniciar un nuevo ciclo infeccioso.
“¿Qué hicimos? Estudiar los patógenos extraídos mediante un proceso estandarizado de purificación de bacterias intracelulares. Con esto logramos extrapolar lo que posiblemente ocurre cuando la bacteria está infectando las células de una vaca”, manifestó Altamirano.
Después de esas 48 horas de incubación de las bacterias en células epiteliales, la científica vio que los microorganismos que salían tenían una mayor capacidad para generar un mejor ciclo de infección.
De esa forma se llegó al resultado principal: el cómplice en desencadenar una respuesta molecular en Brucella abortus, el cual aumenta su potencial infeccioso, es el paso intracelular.
Ahí la bacteria activa los genes que participan en su liberación de las células, y aumenta la expresión de los reguladores que le otorgarán una interacción más eficiente con las nuevas células a contagiar.
Cambio de paradigma
Desde la voz de Michael Schmidt, la investigación también sirvió para debilitar la creencia de la necesidad de una única bacteria de B. abortus para generar la infección.
Con el aporte de Pamela, actualmente hay un mayor fundamento científico de que, entre más bacterias se adhieran a las nuevas células a infectar, más posibilidad hay de iniciar un nuevo ciclo de infección con mayor eficiencia.
“Se tenía el típico pensamiento de que una bacteria de Brucella era suficiente para causar una infección en un ser humano adulto, por ser en extremo infecciosa. Por esta razón, en los Estados Unidos no podemos estudiarla sin el respectivo permiso. Esto hace que el modelo propuesto desde Costa Rica nos aporte en ese entendimiento”, argumentó Schmidt.
Con los hallazgos vigentes y al entender los mecanismos que usa la bacteria para generar infección, a largo plazo se puede usar dicho conocimiento en la generación de tratamientos y vacunas.
“La brucelosis genera grandes pérdidas económicas. Un ganadero que tenga pérdidas en la producción de leche o deba sacrificar su ganado debido a una infección por brucelosis, tiene una gran impacto económico. Por lo tanto, si logramos determinar cómo hace la bacteria y cuáles sistemas necesita para establecer este ciclo de vida celular, estamos más cerca de hallar vacunas más eficientes u otras formas para evitar el establecimiento de esta enfermedad”, concluyó Altamirano.
Usted puede leer el artículo científico completo en:
https://journals.asm.org/doi/10.1128/IAI.00004-21.

Periodista, Oficina de Divulgación e Información
Área de cobertura: ciencias de la salud
jenniffer.jixvrdmenezcordoba @ucrrdpr.ac.cr
Comentarios:
Artículos Similares:
-
 La UCR le aporta al país un estudio sobre zonas de amenaza por inundación
La UCR le aporta al país un estudio sobre zonas de amenaza por inundación -
 Costa Rica recibirá a uno de los expertos internacionales más respetados en el estudio del cáncer
Costa Rica recibirá a uno de los expertos internacionales más respetados en el estudio del cáncer -
 Viróloga de la UCR gana el máximo premio de Biocientífica 2024 por su excelencia profesional
Viróloga de la UCR gana el máximo premio de Biocientífica 2024 por su excelencia profesional -
 La neurociencia y la didáctica del inglés se unen en una experiencia costarricense valorada en …
La neurociencia y la didáctica del inglés se unen en una experiencia costarricense valorada en …
© 2025 Universidad de Costa Rica - Tel. 2511-4000. Aviso Legal. Última actualización: septiembre, 2025